文章亮点
1. 在这项研究中,作者研究了具有不同程度电负性的三价金属碳化物,并通过实验合成了 Sc2C。
2. 作者将材料确定为二维 (2D) 电子化物,尽管 Sc比之前在电子化物位点附近发现的任何金属都更具电负性。
3.通过计算 Sc2C和 Al2C,作者发现阳离子的更高电负性驱动金属和电子轨道之间的更大杂化,这在这些材料中打开了带隙。
4. Sc2C 是第一个二维电子半导体,作者提出了阳离子电负性驱动其能带结构变化的设计规则。
背景介绍
能量存储、电子学和催化领域的挑战促使人们寻找具有极端特性的奇异材料,而在化学计量浓度-俘获裸电子的电化物晶体具有一些最卓越的特性。这些电子已从原子轨道中弹出以驻留在空晶格位置,并且由于它们的结合非常弱,是比碱金属更好的电子供体,可以提供与银相媲美的电导率,并且可以催化具有挑战性的反应。
这些特性导致在需要富电子材料的应用中探索电子化合物:N2 和 CO2 还原、电池电极、和电子发射器。尽管取得了这些进展,但可能预测电子化合物的规则基于其结构或组成的特性不发达。例如,与传统材料不同,不知道如何调整电子化合物的带隙。而且,更关键的是,可以预测材料是否为电子化合物的简单规则仍然不精确。
目前,只有两个预测电子化合物的规则被广泛接受:
(1) 在电子化合物电子周围形成配位球的金属原子必须是正电的并且
(2) 化合物必须是富电子的。
例如,在 [Ca2N]+(e-) 中,钙是正电的,并且该化合物是富电子的,因为首选的氧化态 (Ca2+,N3−) 和化学计量提供额外的电子,形成电子化物。然而,这些规则过于宽泛,因为许多化合物满足这些规则但不是电子化合物。为了改进这些规则,实验已经开始识别可以与电子相邻的金属。到目前为止,只有 Ca、Sr、Ba、Y、Hf、和 Gd被掺入到 electride 站点旁边(图 1),而 Sc 和一些镧系元素已在计算上被确定为候选者。最近在 Ca5Pb3(非电子化合物)和 Ca3Hf2Pb3(电子化合物)的情况下探索了电子计数和电负性之间的这种微妙平衡,因为用铪代替钙使化合物富电子。
尽管有这些发现,但阳离子电负性在形成电子产品尚不为人所知。因此,为了改进电子化合物的设计规则及其结构-性能关系,作者探索了具有层状结构的三价金属碳化物。这个族的信息量很大,因为 Y2C 是一种已知的电子化合物,Sc2C 已被预测,而 Al2C 是未知的,此外,这些金属在电负性方面系统变化(图 1)。
电负性问题是必不可少的,因为实验观察到的两种电子化合物 Y2C和 Hf2S 是“混合”电子化合物,其中电子化合物的电子与相邻的金属轨道有一些重叠,金属的电负性可能与杂化程度相关。这种共价键在定义电子结构的电子结构中起着重要作用,因为电子通常位于费米能级附近。
因此,随着杂化的发生,可调带结构成为可能,实际上,Y2C是一种半金属。虽然有零维 (0D) 电子化物和富电子半导体的例子,但这种半金属特性在二维 (2D) 电子化物中是独一无二的。这种特性引发了一个问题,即是否更高程度的杂化金属和电化物电子之间的关系可能会导致新类别的电化物材料。
这些问题激发了作者探索 M2C 系统,尤其是层状 Sc2C 的动力。为了突出Sc2C 系统中的不确定性,作者简要概述了以前的发现和预测。
Sc2C 最初是在1967 年合成的,属于 NaCl 结构类型,作者在下文中将其称为立方相。1969 年,根据其粉末 X 射线衍射 (PXRD) 将该结构重新指定为层状 (R3̅m) ) 模式,即使该模式缺少几个重要的反应。1989 年,该结构再次被重新指定为立方相(图 2a,根据作者的发现进行了更新)。该分配似乎是正确的,并且不知道是否存在分层的 Sc2C 电子化合物。目前,2D Sc2C MXene 结构已在计算上进行了探索,并且计算预测层状 Sc2C将是一种电子化合物。此外,2D Sc2C 已被预测可储存 8% 重量的氢并可逆地储存氟化物作为电池阳极的容量超过了最先进的锂离子电池。
因此,如果确实存在分层的 Sc2C电极,它可以实现这些令人兴奋的预测。在这项研究中,作者使用进化算法预测分层 Sc2C是稳定的,并通过实验探索所需成分周围的相图。然后作者计算合成材料的电子结构并将其与 Y2C 和 Al2C 进行比较以了解周期性趋势。发现随着阳离子变得更加带负电,带隙打开,Y2C 作为半金属,Sc2C作为小带隙半导体,Al2C 作为更大的带隙半导体。合成的层状 Sc2C是第一个具有半导体特性的二维电子化物,开辟了一类令人着迷的新型电子化物材料,在能量存储或光电子学中具有多种可能的应用。
图文速读

图1 调整后的周期表突出了各种阳离子的化合价。鲍林电负性值显示在每个元素符号下方,灰色块表示哪些阳离子已通过实验结合到电子化物位点旁边。列出了潜在电子的预测特征,并说明了电子-原子杂化。

图2
(a) 二元 Sc-C 相图, 包括层状 Sc2C 相(红色)。
(b) Sc-C 相的赫尔图,使用 USPEX 计算。显示了层状 Sc2C(红色)、立方 ScCx(蓝色)和 α-Sc4C3(紫色)的常规晶胞。

图3 与计算的层状和立方 Sc2C 相相比,实验结构的 X 射线衍射图。层状和立方体的计算量显示为通过 Rietveld 方法确定。比较了预测的和实验的晶格参数。

图4
(a) 退火前 Sc2C的高分辨率透射电子显微镜 (TEM) 图像,彩色晶格平面对应于通过 FFT 确定的不同微晶区域。
(b) Sc2C退火 7 天后的高分辨率 TEM 图像,单晶区域的晶格面为绿色。
(c) [14 7 1] 区轴的选区电子衍射 (SAED) 图案。比较了相应的实验 d 间距。
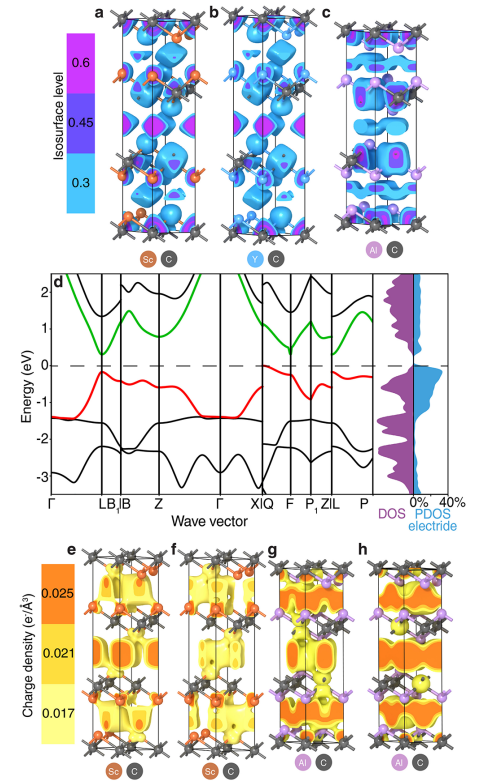
图 5 x=0和1.6样品在298 K下对MeCN蒸汽的吸附等温线。
(a) Sc2C 的三维 (3D) ELF,其中等值面水平的梯度范围从 0.3 到 0.6。这个比例对于每个 ELF 都是相同的。
(b) Y2C 的 3D ELF。
(c) Al2C 的 3D ELF。
(d) Sc2C 能带结构、状态的总密度(紫色)和电子态的部分密度占总数的百分比(蓝色)。价带和导带分别以红色和绿色突出显示。
(e) L 点处 Sc2C价带的电荷密度。电荷密度梯度从 0.017 到 0.025 e-/Å3。这个比例对于每个电荷密度都是相同的。
(f) L 点处 Sc2C导带的电荷密度。
(g) L点处 Al2C 价带的电荷密度。
(h) L 点处 Al2C 导带的电荷密度。

图 6
(a) 不同氧化量后的 X 射线衍射图。
(b) 衍射图案在 54-56° 2θ 之间放大。
(c) 衍射图案在 32.4-33.4° 2θ 之间放大。

图 7 制成的钪和碳在空气中放置 1 天后和在空气中放置 11 天后的 X 射线光电子能谱。
结论与展望
总之,作者合成了一种新的二维无机电子化合物 Sc2C,它是第一个半导体二维电子化合物。在 Sc-C 相图的无序岩盐区域内发现该相表明,一般而言,在许多二元相图的岩盐区域内可能会发现其他新的电子化合物。随着作者对 Al2C 的探索,三价金属碳化物为半导体二维电极带来了新的设计规则,即二维电极中更多的负电阳离子导致更高程度的杂化,从而导致价带和导带的更大分裂。因此,基于阳离子的电负性,作者预测这些电子化物材料中的带隙可能是可控的。这是第一个半导体二维电子化合物的例子,表明它可能用作催化剂或光催化剂,其中电子化合物已经很出色的给电子特性可以通过光激发进一步增强。在 Sc2C 的情况下,它的小带隙特别允许用作红外 (IR) 光电探测器。这些和其他应用——例如,在储氢或作为氟离子电池电极——现在可以进行实验探索。









暂无评论
发表评论